牛津大学团队推出全球首个心脏传感基础模型CSFM,能统一分析智能手环、心电图等多源数据,无论信号来自何处、是否完整,都能精准诊断房颤、预测死亡风险、重构血压波形,甚至用单一脉搏波生成完整心电图。打破了设备壁垒,让偏远地区也能享用顶级心脏监护,推动全球医疗平权。
心血管疾病持续作为全球医疗健康负担的「头号杀手」。如今,心脏信号的采集无处不在——从重症监护室(ICU)的复杂监护仪,到普通病房的十二导联心电图,再到我们手腕上的智能手表。
然而,这些设备产生的数据格式「四分五裂」,通道数各异。这导致现有的医疗人工智能变成了一次性的「定制款」:在医院高精度设备上训练的顶尖模型,一旦换到居家智能手环上,就会因为「水土不服」而彻底失效 。
为了彻底打破这一硬件与数据壁垒,牛津大学Xiao Gu博士与David A. Clifton教授领导的国际联合研究团队,重磅推出了首个多模态心脏传感基础模型(Cardiac Sensing Foundation Model, 简称CSFM。

论文链接:https://www.nature.com/articles/s42256-026-01180-5
该研究成果凭借其极具突破性的视野,被权威顶级学术期刊《Nature Machine Intelligence》遴选为2026年2月刊的封面文章。

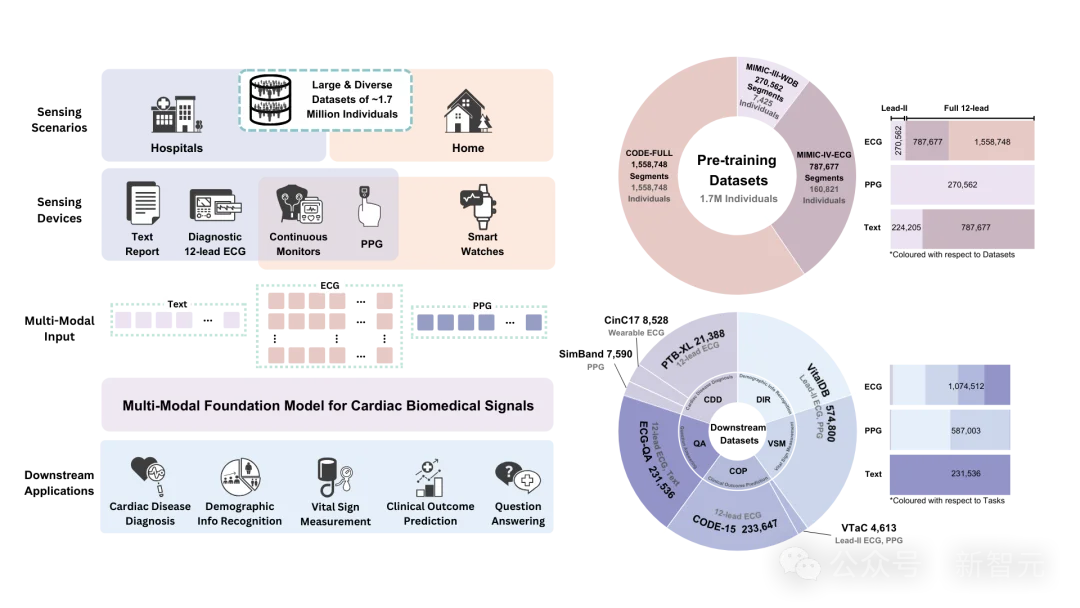
传统AI模型最大的软肋在于「通道依赖」。
CSFM颠覆了这一传统,它通过强大的Transformer架构和创新的「统一词元化(Tokenization)」策略,实现了真正的降维打击。
不论输入的是电压波动的心电图(ECG)、光学反射的脉搏波(PPG),还是医生手写的临床诊断文本;也不管数据是残缺的单导联还是完整的12导联,CSFM都能一视同仁,将它们送入同一个极高维度的「大脑」中进行联合分析。
更惊艳的是,CSFM在预训练时采用了极度苛刻的「掩码自监督学习」——随机抹去75%的信号数据。在「管中窥豹」的极限条件下,模型被逼迫着去真正理解心脏深层的电生理流形与血液动力学规律,而非进行简单的数学插补。这种对高达170万个体异构数据的海量吞吐,赋予了CSFM无与伦比的泛化能力。
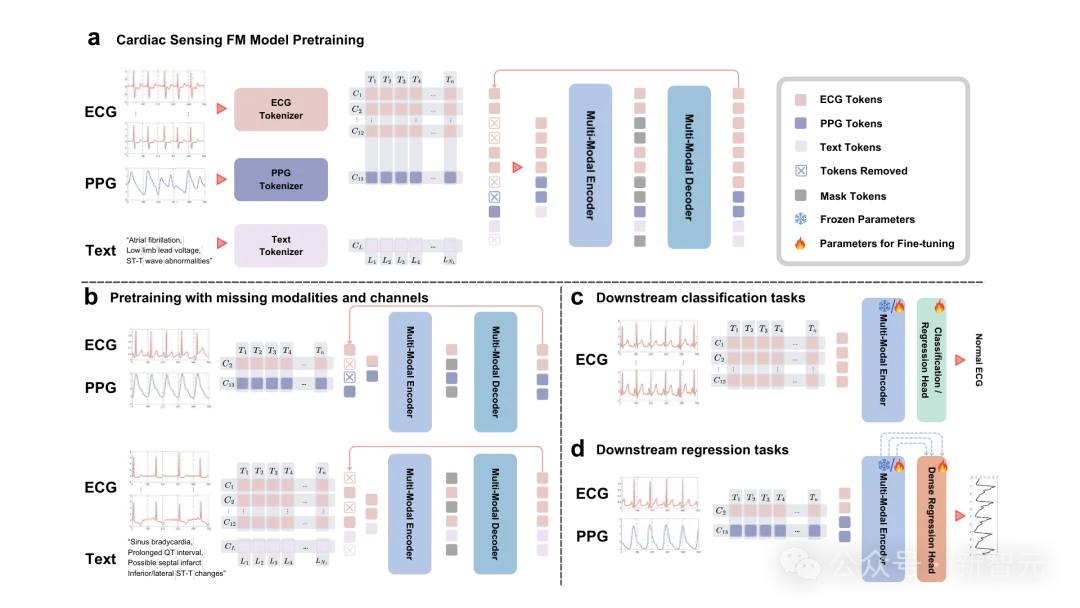
CSFM不是停留在纸面上的理论,它在横跨北美、欧洲及亚洲的真实世界数据集中,接受了五大核心场景的严苛测试,表现全面超越传统的深度学习模型:
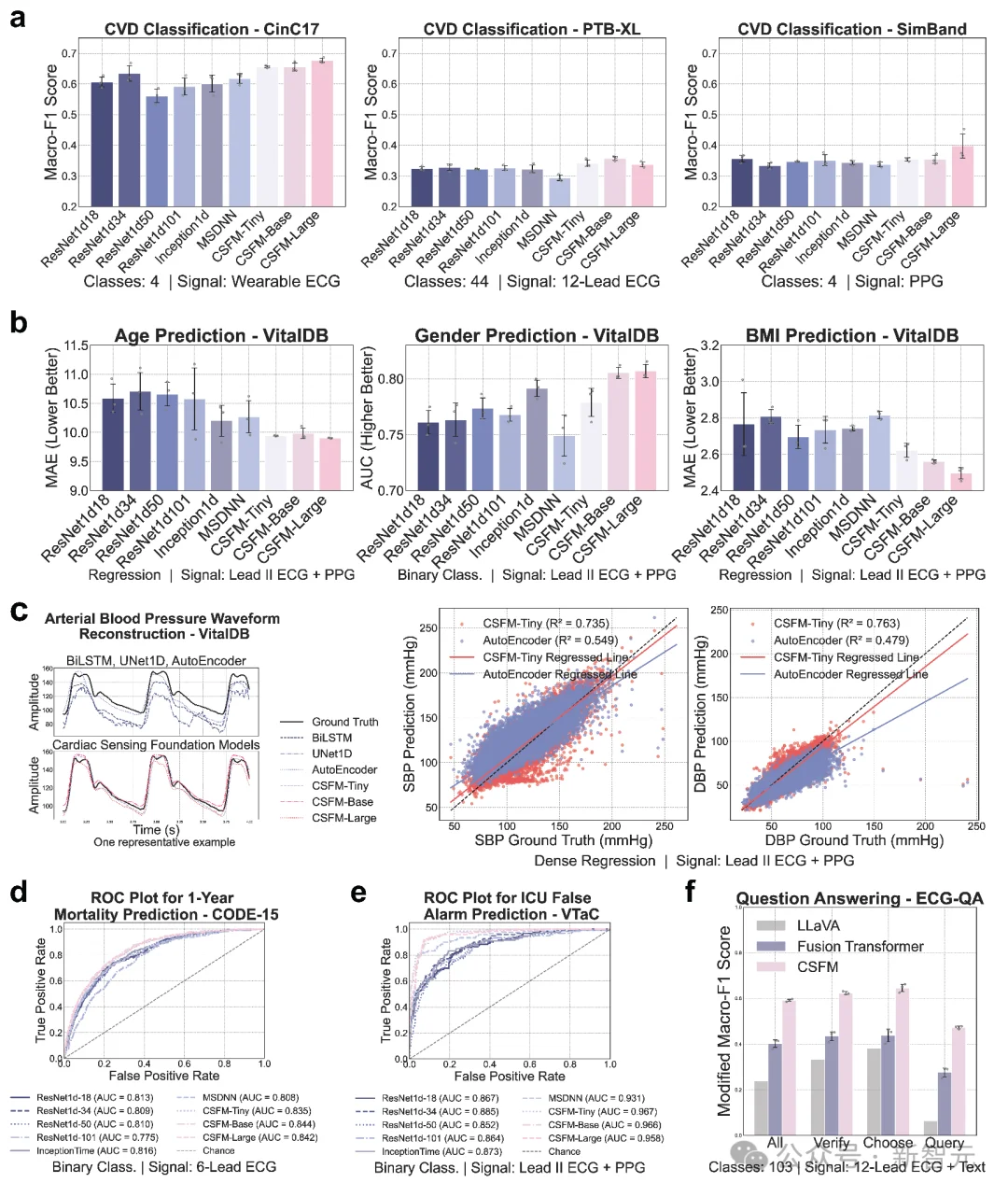
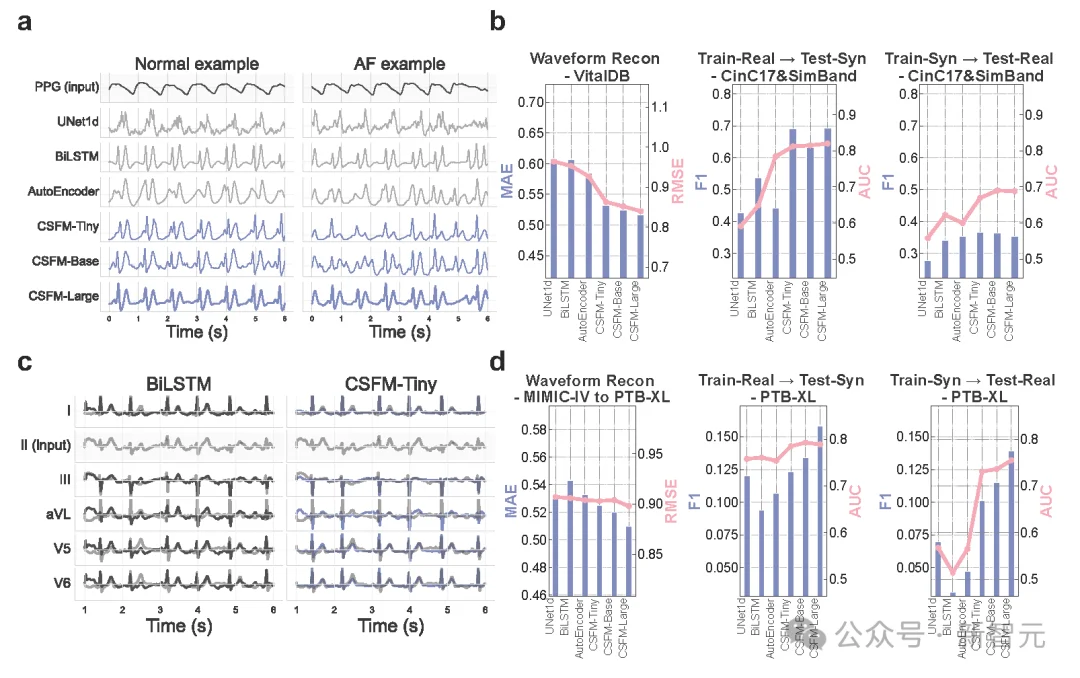
如果说诊断是基础,那CSFM的「跨模态脑补」能力则堪称魔法。在缺乏高端心电图设备的偏远地区或居家环境中:
光学PPG无中生有生成ECG: 仅靠普通消费级智能手环监测到的平缓血流容积光反射变化,CSFM就能跨物理域,重构出具有医疗级保真度的心电图波形(包含清晰的P-QRS-T波群) 。
单导联推演全息12导联: 即使只给CSFM看一根导联的残缺信号,它也能精准推演出包含胸前与肢体完整视角的12导联全息心电2。
对于数字医疗产业而言,CSFM的最大价值在于它是一个「开箱即用」的终极特征提取器。未来的医疗硬件初创公司或一线临床医生,彻底摆脱了搭建庞大算力集群的枷锁。只需调取CSFM的深层特征接口,利用几十个病例和一台普通笔记本电脑,几秒钟内就能训练出极其强大的专病辅助诊断工具。
CSFM的成功不仅是算法性能的一次狂飙,更是数字健康全产业链底层逻辑的重塑。它彻底打破了硬件孤岛与模态壁垒,让无论身处三甲ICU还是偏远山区的患者,只需一枚廉价的智能手环,就能随时接入顶级的智能心脏监护网络。
科技向善,CSFM正让全球心脏医疗健康平权迈出历史性的一步!
参考资料:
Gu, X., Tang, W., Han, J. et al. Cardiac health assessment across scenarios and devices using a multimodal foundation model pretrained on data from 1.7 million individuals. Nat Mach Intell 8, 220–233 (2026).
文章来自于“新智元”,作者 “LRST”。